O que aconteceu
Em 18 de abril de 2026, o presidente dos Estados Unidos Donald Trump assinou uma ordem executiva intitulada "Advancing Breakthrough Mental Health Treatments", determinando que a FDA (Food and Drug Administration) e a DEA (Drug Enforcement Administration) acelerem o processo de aprovação e acesso a tratamentos psicodélicos, com foco especial em veteranos de guerra com TEPT (Transtorno de Estresse Pós-Traumático) e depressão resistente. A ordem cria mecanismos administrativos para contornar os gargalos regulatórios que atrasaram aprovações anteriores, como a rejeição do MDMA pela FDA em agosto de 2024, e sinaliza uma mudança de postura institucional sem precedentes em relação aos psicodélicos terapêuticos.
Medidas concretas da FDA (24 de abril de 2026)
Em resposta direta à ordem executiva, a FDA anunciou em 24 de abril de 2026 a emissão de vouchers de revisão prioritária (Commissioner's National Priority Vouchers, CNPVs) para três programas clínicos com psicodélicos. Esses vouchers comprimem o prazo de análise regulatória de 10 a 12 meses para 1 a 2 meses após a submissão do pedido de aprovação (NDA). Os três programas beneficiados são:
- Compass Pathways (COMP360): psilocibina sintética para depressão resistente ao tratamento (TRD). A Compass concluiu dois ensaios Fase 3 com resultados positivos — COMP005 (junho/2025) e COMP006 (fevereiro/2026) — com mais de 1.000 participantes. A empresa prevê submissão do NDA no Q4/2026 e decisão FDA no Q1-Q2/2027. Com o CNPV, a revisão pode ser concluída em 1 a 2 meses após a submissão.
- Usona Institute: psilocibina para depressão maior (MDD). Ensaio Fase 3 em andamento; a Usona confirmou ao Reuters o recebimento do voucher e estima revisão de 1 a 2 meses após a submissão do pedido.
- Otsuka Pharmaceutical / Transcend Therapeutics: methylone (TSND-201) para TEPT. A Otsuka, uma das maiores farmacêuticas do mundo em psiquiatria (fabricante do Abilify/aripiprazol), está adquirindo a Transcend por US$ 700 milhões — aposta institucional de grande porte no setor psicodélico.
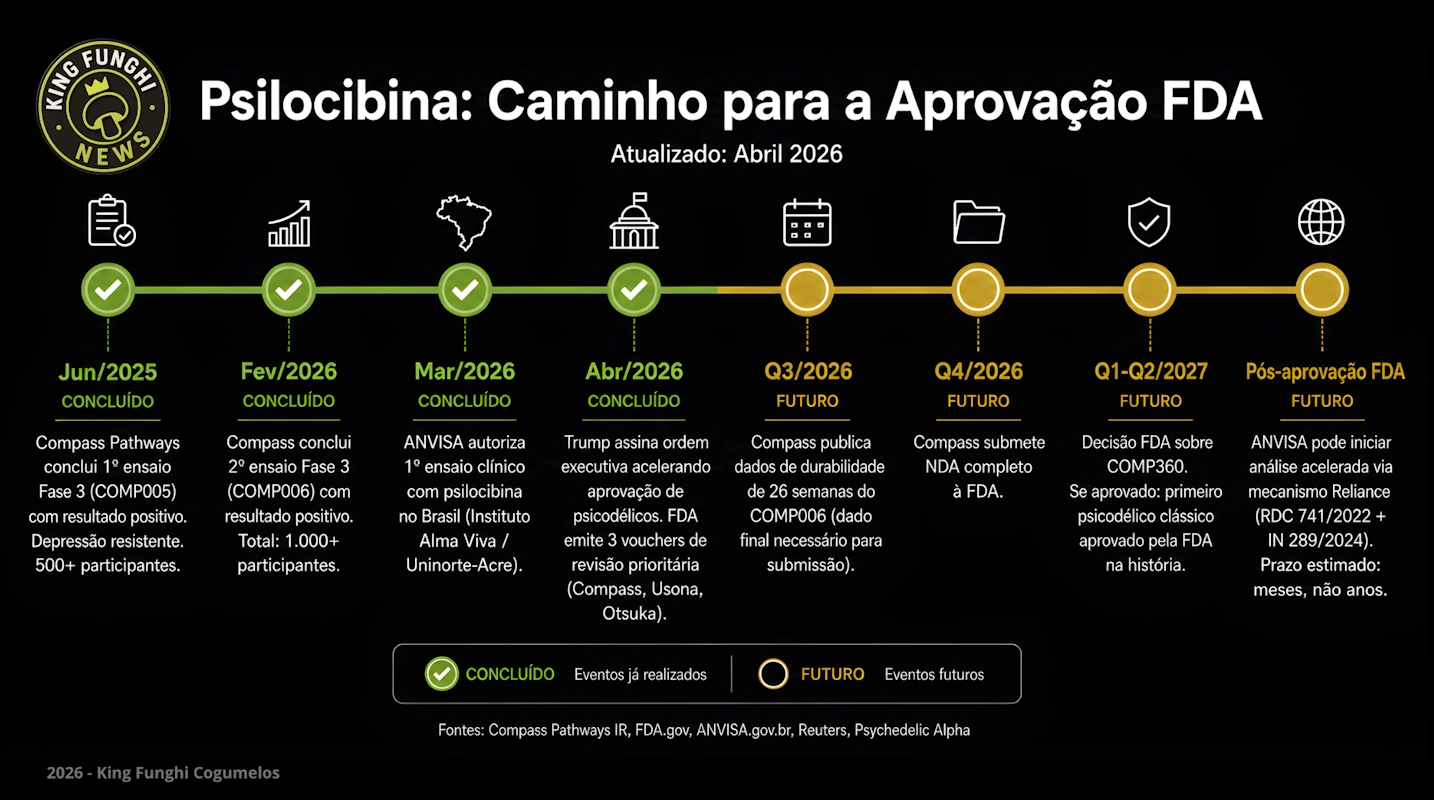
Infográfico: Psilocibina — Caminho para a Aprovação FDA | King Funghi News, Abril 2026
A FDA também anunciou a criação de um grupo de trabalho dedicado exclusivamente a psicodélicos terapêuticos, com prazo de 90 dias para apresentar um roteiro regulatório. Os vouchers podem ser transferidos ou vendidos a outras empresas farmacêuticas, o que abre espaço para que grandes grupos como Pfizer, Roche ou Bayer adquiram esses direitos e acelerem ainda mais o processo.
Contexto: por que isso é relevante
A psilocibina permanece classificada como substância Schedule I nos EUA (sem uso médico reconhecido, alto potencial de abuso) desde 1970. A ordem executiva de Trump não muda essa classificação diretamente, mas cria pressão institucional e mecanismos administrativos concretos para acelerar o processo. Diferente da rejeição do MDMA em 2024, os dados da psilocibina são mais robustos: a Compass acumula dois ensaios Fase 3 positivos consecutivos, com mais de 1.000 participantes e efeitos que persistem por pelo menos seis meses após uma única sessão.
O foco em veteranos é estratégico: segundo o 2025 National Veteran Suicide Prevention Annual Report do U.S. Department of Veterans Affairs (publicado em março de 2026, com dados de 2023), uma média de 17,5 veteranos morrem por suicídio diariamente nos EUA (6.398 mortes em 2023), e os tratamentos convencionais para TEPT têm eficácia limitada nessa população. Estudos da Johns Hopkins, do Imperial College London e da NYU documentam taxas de remissão significativamente superiores com psilocibina em comparação com antidepressivos convencionais.
Impacto para o Brasil
A movimentação americana tem implicações diretas e mensuráveis para o Brasil, em dois planos distintos: o regulatório e o político.
O mecanismo ANVISA que muda o jogo
A ANVISA mantém um sistema formal de "Confiança Regulatória" (Reliance), regulamentado pela RDC 741/2022 e pela Instrução Normativa 289/2024. Esse mecanismo permite que a agência utilize as avaliações de Autoridades Reguladoras Estrangeiras Equivalentes (AREEs) como base para análise acelerada de novos medicamentos no Brasil, reduzindo o prazo de registro de anos para meses. A FDA dos EUA é explicitamente uma das oito AREEs reconhecidas pela ANVISA para registro de medicamentos, vacinas e produtos biológicos.
O que isso significa na prática: se a Compass Pathways, a Usona Institute ou a Otsuka obtiverem aprovação FDA para um medicamento à base de psilocibina, a ANVISA poderá utilizar essa aprovação como fundamento para uma análise otimizada do mesmo produto no Brasil. A agência não é obrigada a fazê-lo, mas o mecanismo existe, é formal e já foi usado para outros medicamentos. A aprovação pela FDA, conhecida mundialmente pelo rigor de seus processos, eliminaria o principal argumento técnico para bloqueio: a ausência de evidências de segurança e eficácia validadas por autoridade competente.
O Brasil já está em movimento
Em março de 2026, a ANVISA autorizou o primeiro ensaio clínico com psilocibina no país, conduzido pelo Instituto Alma Viva em parceria com a Uninorte-Acre, com pacientes oncológicos com ansiedade existencial. É o primeiro uso legal e controlado de psilocibina em pacientes brasileiros. Esse precedente interno, somado à aprovação FDA que se aproxima, cria uma trajetória regulatória que será difícil de ignorar.
O que o governo brasileiro poderia alegar, e o que não poderia
Com uma aprovação FDA em mãos, os argumentos disponíveis para bloqueio se reduzem drasticamente. Restariam, essencialmente, dois: (1) alegação de que o produto aprovado nos EUA não foi testado na população brasileira, o que é tecnicamente fraco dado o padrão de aceitação de dados internacionais pela ANVISA; e (2) resistência política baseada em estigma, que é o argumento mais provável, mas o mais difícil de sustentar publicamente diante de uma aprovação FDA e de dados de segurança robustos.
O precedente mais próximo é o da cannabis medicinal: a ANVISA resistiu por anos, mas a combinação de aprovações internacionais, pressão de pacientes e dados científicos acumulados tornou o bloqueio insustentável. A psilocibina segue a mesma trajetória, com a diferença de que o processo está ocorrendo em velocidade significativamente maior. A movimentação americana, somada às aprovações regulatórias na Austrália (2023), Nova Zelândia (2025) e República Tcheca (2026), cria pressão regulatória global que o Brasil terá crescente dificuldade de ignorar. A trajetória mais realista para o país continua sendo o modelo ayahuasca: regulamentação via CONAD para uso terapêutico em contextos controlados, sem necessidade de aprovação legislativa. O precedente americano fortalece os argumentos técnicos e políticos para essa via.
O que é o mecanismo ANVISA Reliance?
Reliance (ou Confiança Regulatória) é o mecanismo pelo qual a ANVISA pode utilizar, total ou parcialmente, as avaliações de agências estrangeiras reconhecidas para acelerar o registro de medicamentos no Brasil. Está regulamentado pela RDC 741/2022 e pela Instrução Normativa 289/2024. Em vez de conduzir uma análise do zero, a ANVISA aproveita o trabalho já realizado por agências de alta credibilidade, reduzindo o prazo de registro de anos para meses.
A FDA dos EUA é uma das 8 Autoridades Reguladoras Estrangeiras Equivalentes (AREEs) reconhecidas pela ANVISA para registro de medicamentos, vacinas e produtos biológicos. Uma aprovação FDA não obriga a ANVISA a agir, mas cria o caminho formal para análise acelerada.
| Agência | País / Bloco |
|---|---|
| FDA — Food and Drug Administration | EUA |
| EMA — European Medicines Agency | União Europeia |
| Health Canada | Canadá |
| MHRA — Medicines and Healthcare products Regulatory Agency | Reino Unido |
| PMDA — Pharmaceuticals and Medical Devices Agency | Japão |
| Swissmedic | Suíça |
| TGA — Therapeutic Goods Administration | Austrália |
| WHO PQT — World Health Organization Prequalification | Internacional |
Fonte: ANVISA — Confiança Regulatória (Reliance), atualizado em fev/2026
Fontes
- Casa Branca — Comunicado oficial da ordem executiva (18/04/2026)
- FDA — Comunicado de resposta à ordem executiva (24/04/2026)
- Reuters — "US FDA moves to fast-track psychedelic drugs after Trump order" (24/04/2026)
- The Guardian — "Trump signs executive order on psychedelic medication" (24/04/2026)
- Compass Pathways — Comunicado oficial sobre NDA e voucher FDA (24/04/2026)
- Otsuka Pharmaceutical — Aquisição da Transcend Therapeutics por US$ 700 milhões (27/03/2026)
- ANVISA — Confiança Regulatória (Reliance): lista de AREEs reconhecidas
- ANVISA autoriza primeiro ensaio clínico com psilocibina no Brasil (13/03/2026)
O horizonte é favorável. E pode estar mais próximo do que parece.
Os dados são sólidos, o processo regulatório está em movimento e os atores envolvidos são instituições de peso: a FDA americana, a Compass Pathways com mais de 1.000 participantes em ensaios Fase 3, a Otsuka com US$ 700 milhões apostados no setor. Não se trata de promessa ou especulação, mas de uma trajetória documentada.
Se os prazos se confirmarem, uma aprovação FDA para psilocibina pode ocorrer ainda em 2027. A partir daí, o mecanismo ANVISA Reliance cria um caminho formal para que o Brasil siga, com prazo de meses, não anos. O precedente da cannabis medicinal mostrou que a resistência regulatória tem limite quando os dados científicos e as aprovações internacionais se acumulam. A psilocibina está percorrendo esse caminho em velocidade significativamente maior.
Para milhões de pessoas com depressão resistente, TEPT e outras condições para as quais os tratamentos convencionais falharam repetidamente, isso representa algo concreto: a perspectiva real de acesso a um tratamento com eficácia comprovada, seguro quando administrado em contexto clínico controlado, e que produz efeitos duradouros a partir de uma única sessão. Não é uma promessa. É o que os dados mostram.
As próximas notícias sobre esse tema podem ser históricas. Quando a FDA se pronunciar, quando a Compass submeter o NDA, quando a ANVISA der o primeiro passo formal, você vai querer saber antes de todo mundo.
Preencha o formulário abaixo e receba atualizações diretamente no seu e-mail e WhatsApp. Sem spam. Só o que importa, quando importa.



